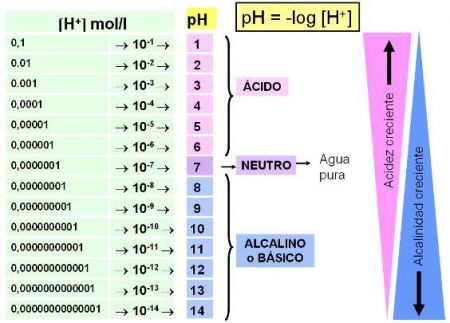
El parámetro pH (poder del hidrógeno) es el indicador de la concentración de iones de hidrógeno [H+]que hay en un líquido. El valor de pH en el acuario marino de arrecife es un parámetro fundamental. Veamos por qué…
La concentración de iones de hidróxido [OH–] es inversamente proporcional a la concentración de iones de hidrógeno. Cuando los iones de hidrógeno son más abundantes la solución es ácida, y cuando los iones de hidróxido son más abundantes la solución es alcalina.
Su fórmula es logaritmo negativo en base 10 de la concentración de hidrogeno:
pH = -Log [H+]
Por cada incremento de una unidad en el pH, la concentración de iones hidrógeno se divide por 10. Por cada decremento de una unidad de pH, la concentración de iones hidrógeno se multiplica por 10.
Es decir, a pH 6 hay 10 veces más H+ que a pH 7, y que a pH 6 hay 100 veces más H+ que a pH 8. En consecuencia, un pequeño cambio en el pH puede significar un gran cambio en la concentración de H+ en el agua.
Visualmente:
Por qué es imporante el pH en el acuario marino de arrecife?
La razón fundamental es que los organismos acuáticos solo prosperan dentro de un rango de pH determinado
El rango considerado como aceptable oscila de 7,8 a 8,5. El valor mínimo del pH debería ser 8,2 y no debería subir de 8,5.
El valor ideal para la calcificación es 8,4
Hay algunos procesos fundamentales como la calcificación de los corales están estrechamente relacionados con el pH. La calcificación disminuye si el pH disminuye.
Además, debemos intentar que nuestro valor de pH sea lo más constante posible, teniendo en cuenta la fluctuación que se da entre el ciclo de día y noche.
Qué hace que caiga el valor de pH en el acuario?
El dióxido de carbono (CO2) que proviene de la atmósfera y de la respiración de animales y plantas es el responsable de la variación del pH.
Cuando se disuelve el CO2 inmediatamente forma ácido carbónico (H2CO3–), de modo que realmente hay poco CO2 en el agua.
CO2 + H2O = H2CO3-
dióxido de carbono + agua = ácido carbónico
El ácido carbónico se disocia en en iones de hidrógeno e ion bicarbonato (HCO3-) lo que resulta en un incremento de iones de hidrógeno perdiendo el equilibrio y produciendo una reacción de acidificación
H2CO3- = H+ + HCO3-
ácido carbónico = hidrógeno + bicarbonato
Y lo iones bicarbonato se disocian a su vez en ion hidrógeno e ion carbonato (CO3), produciendo un desequilibrio mayor y por tanto una mayor acidificación.
HCO3- = H+ + CO3
bicarbonato = hidrógeno + carbonato
Por tanto, una adición de dióxido de carbono desencadena una serie de reacciones que tienen a la acidificación de agua. Pero estas fórmulas son reversibles, así que el consumo del dióxido de carbono llevado a cabo por la fotosíntesis de las algas produce el efecto contrario, subiendo el pH
El resumen de las fórmulas es como sigue:
CO2 + H2O = H2CO3-
dióxido de carbono + agua = ácido carbónico
H2CO3- = H+ + HCO3-
ácido carbónico = hidrógeno + bicarbonato
HCO3- = H+ + CO3
bicarbonato = hidrógeno + carbonato
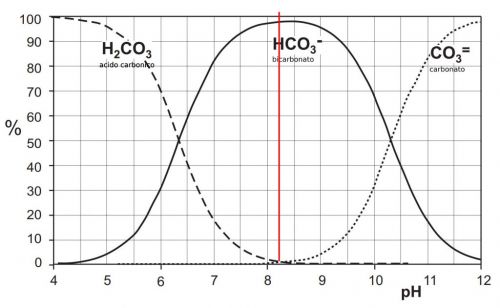
Por tanto se puede establecer el nivel de ácido carbónico, bicarbonato y carbonato en función del nivel de pH según este gráfico:
Podemos ver que con un pH de 8,2 (línea roja) la mayor parte disponible será el bicarbonato
El parámetro que gobierna estos desplazamientos es la alcalinidad, que podemos ver en su entrada correspondiente dentro de este mismo blog.
Muchas de las algas satisfacen su necesidad de carbono del CO2 disponible. Esto es también así para las zooxantelas que viven en los corales, pueden tomar el carbono del dióxido de carbono como resultado de la respiración del coral o del que se encuentra en el agua, pero cuando la fotosíntesis excede la respiración, la colonia se vuelve autotrófica (lo que ocurre en zonas de arrecife muy bien iluminadas) y el dióxido de carbono libre es insuficiente para mantener la fotosíntesis de la zooxantela y entonces utilizarán el bicarbonato como fuente de dióxido de carbono.
Cómo subir el pH en el acuario marino?
Cómo hemos visto anteriormente la caída del pH se produce básicamente por la presencia de CO2 que desencadena todas las reacciones descritas.
Para evitar las variaciones de pH entre el día y la noche se utilizan los refugios con algas con fotoperiodo inverso, de tal modo que neutralizan el dióxido de carbono durante su fotosíntesis, impidiendo que los iones de hidrógeno se liberen y por tanto se produzca la caída de pH.
Este fotoperiodo inverso no debe superar las 14 horas para que el alga pueda hacer su ciclo biológico sin problemas.
Es muy importante tener el refugio bien mantenido porque en el caso de que el refugio se venga abajo va a liberar una cantidad de nutrientes dificílmente asimilable por el acuario.
Otra manera de evitar la entrada de CO2 en el acuario es con el uso de la cal sodada en la entrada de aire del skimmer. La cal sodada secuestra el CO2 del aire y de este modo no se inyecta en el acuario.
El pH, la alcalinidad, magnesio y calcio están íntimamente relacionados.
En este extracto de Reefkeeping http://reefkeeping.com/issues/2006-06/rhf/index.php vemos la importancia del un pH correcto
A un pH bajo (digamos, 7.8), se pueden mantener concentraciones mucho más altas de calcio y alcalinidad en solución que a un pH más alto (digamos, 8.5). Por esta razón, los acuaristas cuyos acuarios tienen un pH bajo a menudo afirman que no tienen problemas para mantener altos niveles de calcio y alcalinidad, y rara vez eliminan el carbonato de calcio de sus bombas, mientras que otros acuaristas con un pH mucho más alto no entienden por qué no pueden mantener tales niveles. condiciones en su acuario, o por qué sus bombas a menudo se obstruyen rápidamente pueden calcificarse más rápido a un pH más alto ). Como seguimiento, no asuma que un pH bajo es mejor porque permite un mantenimiento más fácil del calcio y la alcalinidad y obstruye las bombas más lentamente. También es más estresante para muchos corales calcificantes simplemente porque tienen más dificultades para calcificarse a un pH más bajo. Esa mayor dificultad se debe al hecho de que tienen que bombear un protón (H + ) cuando producen carbonato a partir de bicarbonato, y cuanto más bajo es el pH, más H + ya está en solución, y más difícil es bombear el H adicional+
http://reefkeeping.com/issues/2006-06/rhf/index.php
Para completar la comprensión del pH en el acuario marino de arrecife te animo a que visites (si no lo has hecho ya) esta entrada sobre la alcalinidad el acuario marino de arrecife
Espero haberte convencido de lo importante que es tener un valor de pH lo más estable posible